以下、本文になります
環境システム工学研究室
教員
盛満 正嗣(教授)Masatsugu MORIMITSU
DB| 研究分野 | 空気二次電池,電解採取用陽極,電気化学センサ |
|---|---|
| 研究室 | KE-409 |
| TEL | 0774-65-7765 |
| FAX | 0774-65-7765 |
| mmorimit@mail.doshisha.ac.jp |
研究内容
- 水素と酸素で動く革新的二次電池:高エネルギー密度で安全な水素/空気二次電池の開発
- 省エネルギー・低環境負荷のレアメタル・ベースメタルの製造技術:電解採取用陽極の開発
- 環境・医薬・食品・農業分野の分析に用いる電気化学センサ:リン酸水素イオンセンサの開発
主な研究テーマ
1.水素と酸素で動く革新的二次電池:高エネルギー密度で安全な水素/空気二次電池の開発
古くて新しい、空気電池とは?二次電池化への挑戦
電気エネルギーは貯めることが難しいエネルギーで、これを貯蔵し(充電)、必要なときに取り出す(放電)ことができるのが二次電池(蓄電池)です。ハイブリッド自動車に使われているニッケル水素電池や、電気自動車に利用されているリチウムイオン電池は、いずれも充電と放電ができる二次電池ですが、さらに優れた特性を持つ新たな二次電池の開発が、国内外で積極的に進められています。例えば、科学技術振興機構(JST)の先端的低炭素化技術開発(ALCA)において、タイプの異なる新しい二次電池の開発が行われています。私たちが研究開発を進めている水素/空気二次電池も、このALCAに採択されています。一般に空気電池とは、電池に必須である正極、負極、電解液のなかで、正極での反応に大気中の酸素を利用する電池です。すでに、空気一次電池(放電だけが可能な空気電池)は実用化され、補聴器用のボタン型電池として販売されています。また、空気電池を二次電池にするための研究開発は、これまでに国のプロジェクトとして何度も取り上げられてきましたが、残念ながら実用化に至っていません。つまり、空気電池は古くて新しい電池であり、これを二次電池として実現するには、様々な技術的課題を解決する必要があります。現在、私たちが行っている「水素/空気二次電池の開発」プロジェクトは、その大きな壁を乗り越えようとする挑戦と言えます。
水を生成しながら放電し、水を分解して充電する。新しい概念が未来の電池の可能性を拓く!
水素/空気二次電池は、負極に水素吸蔵合金を用いる空気電池です。充電では、電解液中の水を分解しながら、負極に水素を吸蔵し、正極では酸素が発生して大気中に放出されます。放電はこれとは反対に、負極からは水素が放出され、正極では大気から取り込まれた酸素が還元されるのと同時に水素と反応して、水が生成します。つまり、水を分解して充電し、水を生成しながら放電する二次電池です(図1)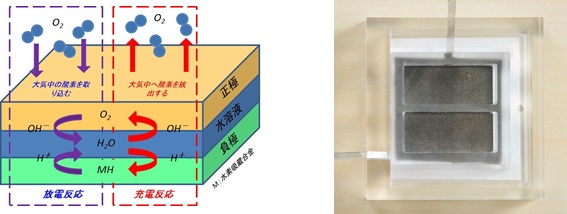
図1 水素/空気二次電池の概念図と開発中の電池写真
実は、このような反応による空気電池を国内で研究しているのは、私たちのALCAプロジェクトだけです。他の大学や研究機関では、負極にリチウムなどの金属を用いる空気電池を研究しています。リチウムのような反応性の高い金属を使うと、電池の起電力が高くなるので良いのですが、空気電池の負極として用いるには多くの課題を抱えています。それは過去の国家プロジェクトの中で空気二次電池が実現できなかった理由と同じで、電池反応に起因する課題であり、極めて解決が困難なものです。一方、水素/空気二次電池は電池反応が全く異なるため、リチウムを用いる場合のような課題はありません。つまり、どのような負極を選択して電池反応を構成するかが、空気電池を二次電池として実現できるかどうかのキーポイントでした。
また、次々世代の二次電池に求められる性能の中で、最も重要なものは高いエネルギー密度です。高いエネルギー密度とは、できるだけ軽く、小さな電池で大きなエネルギーを貯められることを意味しています。このような高エネルギー密度の二次電池が開発できれば、電気自動車はより長い距離を走り、車内空間をより広くとることができます。また、戸建て住宅、集合住宅、商業ビルなどのそれぞれに適した二次電池を設置し、自然エネルギーで発電した電力を貯蔵して必要なときに使うことで、電気エネルギーをより有効に利用することも可能になります。軽く、小さくても大きなエネルギーを貯めることができる二次電池は、このような電気エネルギーの有効利用や省電力に大きく寄与するのです。
さらに、私たちの研究室では電池全体の開発とともに、正極に必要な触媒の開発を行っています。この触媒は、放電のときには大気中の酸素を還元し、充電のときにはアルカリ性水溶液から酸素を発生させるという、2つの反応に対して働く必要があります。これを二元酸素触媒と呼んでいますが、実はいずれの反応もこれまで高い触媒活性を得ることが極めて難しく、この二元触媒の性能が水素/空気二次電池の実現のカギと言えます。私たちの研究室では、水素/空気二次電池の正極に必要な新たな触媒の開発を進めています。
その成果は着実に現れていて、ALCAプロジェクトで開発目標としたエネルギー密度800Wh/L(電池体積1リットル当たりのエネルギー密度)を達成しました。この800Wh/Lという値は、現在最もエネルギー密度が高いリチウムイオン二次電池でも、理論的に達成することが不可能なものです。さらに、1000Wh/Lを超えるエネルギー密度を持つ二次電池はまだ実用化されていませんが、私たちの水素/空気二次電池はその達成も間近な状況にあります。
水素/空気二次電池が優れているのは性能だけでなく、高いエネルギー密度と安全性を両立できる点です。リチウムのような反応性の高い材料を使用せず、電解液に可燃性の有機物を用いることもない二次電池であるからこそ、エネルギー密度と安全性をトレードオフとしない革新的な二次電池の開発が可能となるのです。
この電池を国内で研究開発しているのは、私たちのプロジェクトだけだと書きましたが、実は米国NASAのJPL(Jet Propulsion Laboratory)が、DOE(Department of Energy)による研究費の支援を受けて、平成26年から水素/空気二次電池の研究開発を始めました。今後、水素/空気二次電池の研究開発は、日本から世界へさらに広がるかもしれません。電池開発は厳しい競争の分野として知られていますが、世界初の水素/空気二次電池の実用化を目指していきます。
また、次々世代の二次電池に求められる性能の中で、最も重要なものは高いエネルギー密度です。高いエネルギー密度とは、できるだけ軽く、小さな電池で大きなエネルギーを貯められることを意味しています。このような高エネルギー密度の二次電池が開発できれば、電気自動車はより長い距離を走り、車内空間をより広くとることができます。また、戸建て住宅、集合住宅、商業ビルなどのそれぞれに適した二次電池を設置し、自然エネルギーで発電した電力を貯蔵して必要なときに使うことで、電気エネルギーをより有効に利用することも可能になります。軽く、小さくても大きなエネルギーを貯めることができる二次電池は、このような電気エネルギーの有効利用や省電力に大きく寄与するのです。
高エネルギー密度の実現は触媒技術がカギ!
ALCAプロジェクトでは私が研究開発責任者となり、同志社大学ほか5者が参画した研究開発体制となっています。日本の大学で電池の研究を行う場合、電池を構成する正極、負極、電解液のいずれか1つを取り上げた研究が多いのですが、このプロジェクトでは私たちの研究室で電池の作製と評価を行っています。さらに、私たちの研究室では電池全体の開発とともに、正極に必要な触媒の開発を行っています。この触媒は、放電のときには大気中の酸素を還元し、充電のときにはアルカリ性水溶液から酸素を発生させるという、2つの反応に対して働く必要があります。これを二元酸素触媒と呼んでいますが、実はいずれの反応もこれまで高い触媒活性を得ることが極めて難しく、この二元触媒の性能が水素/空気二次電池の実現のカギと言えます。私たちの研究室では、水素/空気二次電池の正極に必要な新たな触媒の開発を進めています。
その成果は着実に現れていて、ALCAプロジェクトで開発目標としたエネルギー密度800Wh/L(電池体積1リットル当たりのエネルギー密度)を達成しました。この800Wh/Lという値は、現在最もエネルギー密度が高いリチウムイオン二次電池でも、理論的に達成することが不可能なものです。さらに、1000Wh/Lを超えるエネルギー密度を持つ二次電池はまだ実用化されていませんが、私たちの水素/空気二次電池はその達成も間近な状況にあります。
水素/空気二次電池が優れているのは性能だけでなく、高いエネルギー密度と安全性を両立できる点です。リチウムのような反応性の高い材料を使用せず、電解液に可燃性の有機物を用いることもない二次電池であるからこそ、エネルギー密度と安全性をトレードオフとしない革新的な二次電池の開発が可能となるのです。
この電池を国内で研究開発しているのは、私たちのプロジェクトだけだと書きましたが、実は米国NASAのJPL(Jet Propulsion Laboratory)が、DOE(Department of Energy)による研究費の支援を受けて、平成26年から水素/空気二次電池の研究開発を始めました。今後、水素/空気二次電池の研究開発は、日本から世界へさらに広がるかもしれません。電池開発は厳しい競争の分野として知られていますが、世界初の水素/空気二次電池の実用化を目指していきます。
2.省エネルギー・低環境負荷のレアメタル・ベースメタルの製造技術:電解採取用陽極の開発
銅、亜鉛、ニッケル、コバルト…社会を支える金属の製造技術とは?
ベースメタルというのは流通量の多い金属のことで、銅や亜鉛などがその代表です。例えば、銅は電線や電池材料に、亜鉛は電池材料や鋼板の防食被膜として幅広く使われています。これらに比べて、ニッケルやコバルトなどは資源量が少なく高価であり、レアメタルと呼ばれています。しかし、レアメタルも電池やステンレスの材料など、私たちの暮らしの中で様々な用途に使用されています。ベースメタルやレアメタルの製造には電解採取法(図2)が用いられています。これは金属元素を含む鉱石を採掘・粉砕した後、酸で金属イオンを水溶液中に抽出してから、そこに陽極(+極)と陰極(-極)を挿入して電気を流すことで、陰極上に目的の金属を析出させる方法です。このようにして鉱石から高純度の金属が製造されています。電解採取では、通電する電気量(電流×時間)が大きくなれば、得られる金属の量は増えます。一方、電解採取によって世界で一年間に消費される電気エネルギー(電気量×電圧)は、亜鉛だけを例にとっても、日本の一般家庭1100万世帯分が消費する量に相当するほど莫大です。また、これまでの電解採取法では、陽極で金属酸化物が生成するという副反応が起こり、これが水溶液中に沈殿して金属汚泥を生じるという問題もありました。
電解採取は金属の製造に不可欠な技術ですが、新興国の経済発展とともにベースメタルやレアメタルの需要は増加しており、電解採取におけるエネルギー消費や環境負荷の増加は大きな課題となっていました。そこで、省エネルギーと環境負荷の低減を同時に達成できる、新たな製造技術の開発が期待されていました。
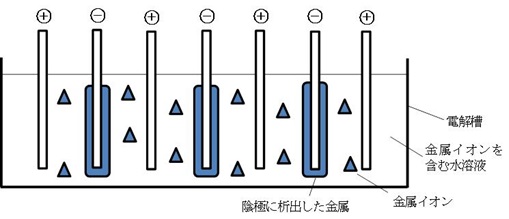
図2 電解採取法の概念図
金属イオン(▲)は陰極(-)で還元され金属となり、陽極(+)では水溶液の電気分解によって酸素または塩素が発生する。一定量の金属が陰極上に析出すると、陰極を電解槽から引き上げ、析出した金属を回収する。これが純金属として様々な用途で使用される。電解槽の長さは数10メートルにもおよび、一つの電解槽に入る陽極や陰極は1,000枚以上となる場合もある。
電解採取プロセスでは陰極で目的とする金属が析出しますが、陽極では酸素または塩素が発生します。このとき陰極の電位は、析出する金属の種類で変わるのですが、陽極の電位は反応が酸素か、塩素かによる違いのみです。例えば、これまでの電解採取では陽極で酸素が発生する場合、鉛合金を材料とする陽極が用いられてきました。しかし、鉛合金は酸素を効率よく発生させるには十分ではなく、また金属汚泥が生じる問題もありました。つまり、これらを解決することができれば、様々な金属の電解採取において、省電力と低環境負荷を同時に達成できると考えました。
従来とは異なる新しい陽極の開発には、酸素や塩素を効率よく発生することができる新しい触媒が必要でした。また、金属汚泥が発生する副反応よりも、優先的に酸素や塩素を発生させる必要もありました。つまり、一定の電流が流れているなかで、陽極の電位が下がって電圧を小さくすることができ、金属汚泥ができる反応 ではなく、酸素や塩素の反応に高い選択性を持つような触媒の開発がターゲットとなりました。
この陽極は導電性を保つための基材としてチタンを使用し、その表面に数ミクロン程度の酸化物触媒層を形成したものです。この構成の電極は酸化物被覆チタン電極と呼ばれ、以前から利用されている分野はありましたが、触媒である酸化物層は従来とは大きく異なっています。私たちが開発した陽極の触媒層は、酸素や塩素の発生に高い触媒活性を持つ酸化物Aと、これらの反応にまったく触媒活性を示さない酸化物Bの混合酸化物であり、酸化物Aは10~20ナノメートル程度の粒子で、このナノ粒子がアモルファス構造の酸化物Bの中に、均一に分散されたハイブリッド構造となっています。このような構成とすることによって、主反応が起こる電位を下げることに成功し、一方で起こってほしくない副反応を効果的に抑制することができました。
ナノ/アモルファスのハイブリッド構造(図3)は、これまで電極に用いられていた酸化物触媒にはなかった新しい概念であり、触媒活性の高い酸化物をナノ粒子とすることで、主反応が起こる面積が大幅に増加するのと同時に、このナノ粒子を反応が起こらない別の酸化物中に分散させることで、副反応をブロックする効果が得られたのです。すなわち、主反応である酸素や塩素の発生は、従来の陽極に比べて触媒活性が10倍以上大きくなり、副反応として知られている二酸化鉛、マンガン酸化物、コバルト酸化物といった金属酸化物の生成は、いずれも抑制することが可能になりました。
このような結果、電解採取の電圧を最大で700mV(図4)、消費電力を36%までそれぞれ削減することに成功し、同時に金属汚泥も発生しない新しい電解採取用陽極が生まれました。これは過去100年にも及ぶ電解採取での金属製造の歴史に、革新的な進歩をもたらすものとなりました。
陽極が解決のカギ!新たな陽極触媒の開発へ
電解採取で消費される電気エネルギーは(電気量×電圧)ですから、電気量が同じでも電圧が小さくなれば、消費されるエネルギーを削減することが可能です。電気量を小さくしても消費エネルギーは下がりますが、これでは生産される金属の量が少なくなってしまいます。生産量を落とすことなく、消費エネルギーを削減するためには電圧を小さくすることが有効です。電解採取の電圧は、一定の電流を陽極と陰極の間に流しているときの2つの電極の電位差になります。このとき陽極の電位のほうが、陰極よりも常に高い値です。つまり、陽極の電位を下げて陰極の電位に近づけることができれば、結果として電圧を小さくすることができます。電解採取プロセスでは陰極で目的とする金属が析出しますが、陽極では酸素または塩素が発生します。このとき陰極の電位は、析出する金属の種類で変わるのですが、陽極の電位は反応が酸素か、塩素かによる違いのみです。例えば、これまでの電解採取では陽極で酸素が発生する場合、鉛合金を材料とする陽極が用いられてきました。しかし、鉛合金は酸素を効率よく発生させるには十分ではなく、また金属汚泥が生じる問題もありました。つまり、これらを解決することができれば、様々な金属の電解採取において、省電力と低環境負荷を同時に達成できると考えました。
従来とは異なる新しい陽極の開発には、酸素や塩素を効率よく発生することができる新しい触媒が必要でした。また、金属汚泥が発生する副反応よりも、優先的に酸素や塩素を発生させる必要もありました。つまり、一定の電流が流れているなかで、陽極の電位が下がって電圧を小さくすることができ、金属汚泥ができる反応 ではなく、酸素や塩素の反応に高い選択性を持つような触媒の開発がターゲットとなりました。
ナノ粒子とアモルファスのハイブリッド!新規触媒による劇的な省電力効果
新たな触媒の開発では、陽極の主反応である酸素または塩素の発生に対しては高い触媒活性があり、金属汚泥の発生という副反応に対しては触媒活性を持たないという、全く反対の特性を同時に満たすことが必要でした。こうした観点から研究を進めた結果、これらの特性を有する触媒を用いた電解採取用陽極と電解採取法を世界で初めて開発しました。この陽極は導電性を保つための基材としてチタンを使用し、その表面に数ミクロン程度の酸化物触媒層を形成したものです。この構成の電極は酸化物被覆チタン電極と呼ばれ、以前から利用されている分野はありましたが、触媒である酸化物層は従来とは大きく異なっています。私たちが開発した陽極の触媒層は、酸素や塩素の発生に高い触媒活性を持つ酸化物Aと、これらの反応にまったく触媒活性を示さない酸化物Bの混合酸化物であり、酸化物Aは10~20ナノメートル程度の粒子で、このナノ粒子がアモルファス構造の酸化物Bの中に、均一に分散されたハイブリッド構造となっています。このような構成とすることによって、主反応が起こる電位を下げることに成功し、一方で起こってほしくない副反応を効果的に抑制することができました。
ナノ/アモルファスのハイブリッド構造(図3)は、これまで電極に用いられていた酸化物触媒にはなかった新しい概念であり、触媒活性の高い酸化物をナノ粒子とすることで、主反応が起こる面積が大幅に増加するのと同時に、このナノ粒子を反応が起こらない別の酸化物中に分散させることで、副反応をブロックする効果が得られたのです。すなわち、主反応である酸素や塩素の発生は、従来の陽極に比べて触媒活性が10倍以上大きくなり、副反応として知られている二酸化鉛、マンガン酸化物、コバルト酸化物といった金属酸化物の生成は、いずれも抑制することが可能になりました。
このような結果、電解採取の電圧を最大で700mV(図4)、消費電力を36%までそれぞれ削減することに成功し、同時に金属汚泥も発生しない新しい電解採取用陽極が生まれました。これは過去100年にも及ぶ電解採取での金属製造の歴史に、革新的な進歩をもたらすものとなりました。

図3 電解採取用陽極に用いられている触媒の電子顕微鏡写真
触媒は二種類の金属酸化物の混合物であり、触媒活性を持たない非晶質酸化物(写真の黒色部分)がマトリックスとなり、触媒活性の高い別の酸化物がこのマトリックス中に10~20ナノメートルのナノ粒子として均一に分散された状態である。
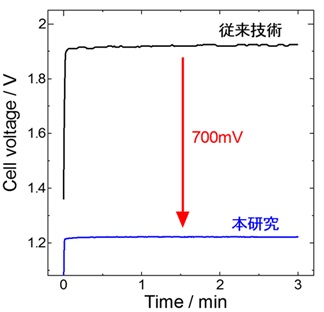
図4 銅電解採取における電解電圧の比較
Morimitsuブランドの世界発信で地球規模のエネルギー・環境問題に応える
私たちの研究成果は国内外に特許出願され、そのうち外国出願は40件以上にも及んでいます。また、電解採取用陽極とこれを用いる電解採取法の特許・ノウハウを、米国のOutotec USA社へライセンシングし、陽極を製造するとともに実際の電解採取プラントでの評価を行ってきました。その結果、メキシコの銅電解採取プラント(年間生産量3万トン)をはじめとする複数のプラントでの実用化に成功し、MSA®(Morimitsu Smart Anode)の登録商標で世界16ヶ国のプラントへの導入が現在進められています。今後5年程度での全面的な導入を予定していて、これが実現すれば100万kW級の原子力発電5基分に相当する電力削減効果が期待されます。さらに、新たに開発した電解採取技術は鉱石からの金属製造だけでなく、これまで廃棄された金属汚泥や家電製品などからの有価金属の回収にも利用できます。このようなリサイクルは高コストであることが大きな課題でしたが、そのブレークスルーとなる技術を提供できると考えています。このように、同志社大学発の技術を世界に浸透させ、社会のなかで役に立つ技術として広く普及させることが重要です。エネルギー・資源の乏しい日本から、この技術を積極的に発信・提案していくことで、地球規模のエネルギー・環境問題に応えていきたいと考えています。
3.環境・医薬・食品・農業分野の分析に用いる電気化学センサ:リン酸水素イオンセンサの開発
リンを迅速に分析できる世界初の電気化学センサを目指して
私たちの研究室では、水素/空気二次電池や金属電解採取の分野で開発された触媒技術を、これらとは分野が大きく異なる電気化学センサに応用する研究も進めています。その一つの例が、リン酸水素イオンセンサの開発です。リンは生活排水、工業排水、農業排水などに含まれており、多様な発生源から環境に放出され、湖沼、河川、沿岸地域の富栄養化をもたらし、赤潮やアオコなどを引き起こす原因となります。また、高濃度のリンが環境水に入ると、その除去には多段階の処理が必要で上水処理が困難であり、飲料水の汚染や品質低下を引き起こします。一方、リンは農作物や食品中の残留農薬を調べる指標であり、食品安全管理のためにその濃度が調べられています。さらに、医療や医薬品開発の分野では、血中のリン濃度の異常による高リン酸血しょうや低リン酸血しょうがあり、これによって呼吸不全や心不全が起こる可能性があります。このように、リンの分析は環境・医薬・食品・農業などの多くの分野で必要な技術です(図5)。しかし、現在の分析方法では、多段階の化学処理と大型の分析装置が必要であり、短時間で正確にリンを分析できる方法が求められていました。私たちの研究室では、迅速かつ高い精度でリンを分析する方法として、リン酸水素イオンをターゲットとする電気化学センサの開発を行っています。これまでリンを測定することができる電気化学センサは実用化されていませんが、その理由には、リンをすばやく、幅広い濃度範囲で、精度よく検出することができる電極触媒がなかったことが挙げられます。私たちはこの要求を満たすことができる新たな触媒の開発に成功し、数十秒でリンを検出して、濃度を測定できることを明らかにしました。この技術を実用化するために、さらに高性能な触媒と、世界初のリンを対象とする電気化学センサの開発を進めています。
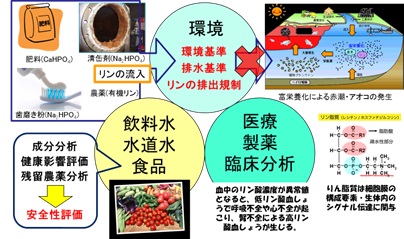
図5 リンのセンシングが必要な分野